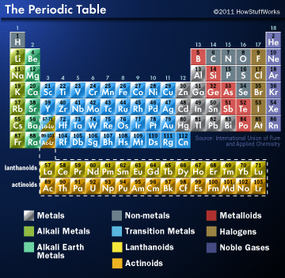
一块一块地构建元素周期表
元素周期表的每一块都包含一个元素,以及关于该元素的一些标准事实:
- 原子序数:等于该元素中质子或电子数量的整数。金的原子序数是79。
- 元素符号:一两个字母。如果是两个字母,第一个总是大写。氢的符号是H,而氦的符号是He。符号可能很棘手,因为有些是基于元素通用名称的第一个字母(s),如氢,而其他符号是基于元素的拉丁名称,如Au代表金(或)金在拉丁语中)。
- 元素名称
- 原子量:通常是十进制值,例如黄金的196.966 569(4)
一些元素周期表包括电子构型(电子的排列)在块的一个角落或在元素名称下面。此外,一些元素周期表还精心设计了彩色符号,以表示元素在标准温度(25摄氏度或77华氏度)下是固体、液体还是气体,以及彩色背景来表示元素的类型(碱金属、碱性)地球金属、非金属、惰性气体等)。
广告
您还记得,在表中,元素是通过增加原子序数来排列的。这些元素横跨7行。每一行称为a期并表示该元素原子核周围的电子所占据的能级或壳层(参见原子是如何工作的).例如,第一个能级最多只能容纳两个电子,所以氢和氦占据周期1。在周期2,第二个能级开始填满。模式仍在继续。周期7中的元素有足够的电子开始填满第七个能级。目前还没有已知的元素有八个能级。
高于第一个能级的每一个能级子层次或轨道.这些轨道分别是s (sharp), p (principal), d (diffuse)和f (fundamental)。但是电子不是按照s→p→d→f的顺序直接填满的,那就太简单了。在一个能级的轨道和它下面的轨道之间有一些重叠。例如,第四个能级的电子按照这个顺序排列:4s,然后是3d,然后是4p。(如果你不能很好地描绘它,美国化学学会有一个元素周期表,可以让你看到不同的电子构型是如何工作的在这里.)
随着原子序数的增加,一个能级被填满,一个新的周期开始了。如果你按照原子序数递增的顺序排列所有元素,周期表就会跨越一张整齐的标准纸。这就是为什么化学家格伦·西博格建议把镧系和锕系元素拉出来,放在桌子下面,使其更紧凑。
最外层能级的电子是参与化学反应的不安定电子。所以当每个新周期开始时,就会有化学性质相似的元素——有一个电子的,有两个电子的,有三个电子的,等等。门捷列夫不可能预测到这种周期性,因为他不知道原子结构。但是这些列呢?