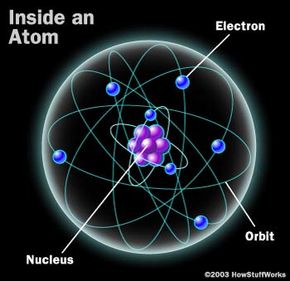
光谱基础知识
光谱学利用所有原子和分子吸收和发射的事实光在某些波长。要了解原因,您必须了解原子的结构。您可以读取原子结构原子如何工作,但这里的快速回顾会有所帮助。1913年,尼尔斯Bohr名字的丹麦科学家占据了欧内斯特卢瑟福的原子模型 - 一个被一个浓密的核心云电子 - 并产生一些稍微改进,更好地利用实验数据。在BoHR的模型中,围绕核的电子存在于离散轨道中,就像绕太阳的行星一样。实际上,我们所有的经典视觉图像都有原子,例如右边的一个原子,在Bohr的概念之后建模。(科学家们自移开了一些BOHR的结论,包括电子在固定路径周围移动的电子概念,而是设想在云中核心聚集的电子。)
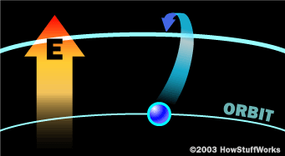
在里面Bohr.原子,特定轨道中的电子与特定的能量相关联。与仍然固定在其轨道上的行星不同,电子可以从一个轨道跳到另一个轨道。其默认轨道中的电子在其上地面州。从地面状态移动到远离核的轨道,电子必须吸收能量。当发生这种情况时,化学家都说电子是一个兴奋状态。电子通常不能无限期地保持兴奋状态。相反,它们跳回到地状态,这一移动需要释放相同的能量,使它们能够首先变得兴奋。这种能量采取了一个形式光子- 在某种波长处,在某种波长处,最小的光颗粒,并且由于波长和颜色与某种颜色有关。
广告
周期性表上的每个元素都有一组唯一的bohr轨道,没有其他元素共享。换句话说,一个元素的电子与另一元素的电子存在略微不同的轨道。因为元件的内部结构是唯一的,所以当它们的电子兴奋时,它们会发出不同的光波长。实质上,每个元素都有一个独特的原子“指纹“采用一组波长的形式,或者光谱。
William Wollaston和Joseph Von Fraunhofer首次开发出来光谱仪看到元素的光谱指纹。光谱仪是一种仪器,它们都展开了光线并显示它进行研究。光进入狭窄的狭缝并穿过透镜,该镜头产生平行光束。这些光线穿过棱镜,弯曲光线。每个波长弯曲略微不同,因此产生一系列彩带。第二透镜将光聚焦在出口狭缝上,这允许一次颜色通过一次通过。科学家们经常使用一个小望远镜,安装在转盘上,观察通过狭缝的颜色更容易。然后,科学家旋转望远镜或棱镜,将另一种颜色带到视野中。通过注意到棱镜的角度或望远镜,可以确定退出光的波长。使用分光镜分析样品可能需要几分钟,但它可以透露大量关于光源。一些光谱仪,称为光谱仪,设置为拍摄频谱。
如您所期望的那样,光谱仪是化学家进行激光光谱的重要工具。接下来,我们将简要介绍一些最重要的激光光谱类型。